|
BIOI 综述丨槲皮素在神经保护中的机制见解和治疗潜力:通路和临床前景
作者:BIOI 来源: 时间:2025-09-10 访问量: 405 |
|
神经退行性疾病(NDDs),比如阿尔茨海默病(AD)、帕金森病(PD)和亨廷顿病(HD),正在成为全球公共健康的巨大负担。它们的共同特征是不可逆的神经元丧失,伴随认知下降、运动障碍和行为改变。然而,目前临床上多数治疗仍以对症支持为主,缺乏能够真正阻止疾病进程的药物。 在这种背景下,研究者将目光投向了天然产物——特别是黄酮类化合物。其中,槲皮素(Quercetin)因其广泛存在于日常食物(如苹果、洋葱、茶叶)中,同时具备强大的抗氧化、抗炎和细胞保护作用,成为“潜力股”。 主要内容 近日,发表于《BIO Integration》的综述《Mechanistic Insights and Therapeutic Potential of Quercetin in Neuroprotection: A Comprehensive Review of Pathways and Clinical Perspectives》,以槲皮素为核心,从分子机制、构效关系(SAR)、药代学特点到临床前景,全面剖析它在神经保护中的多重作用。
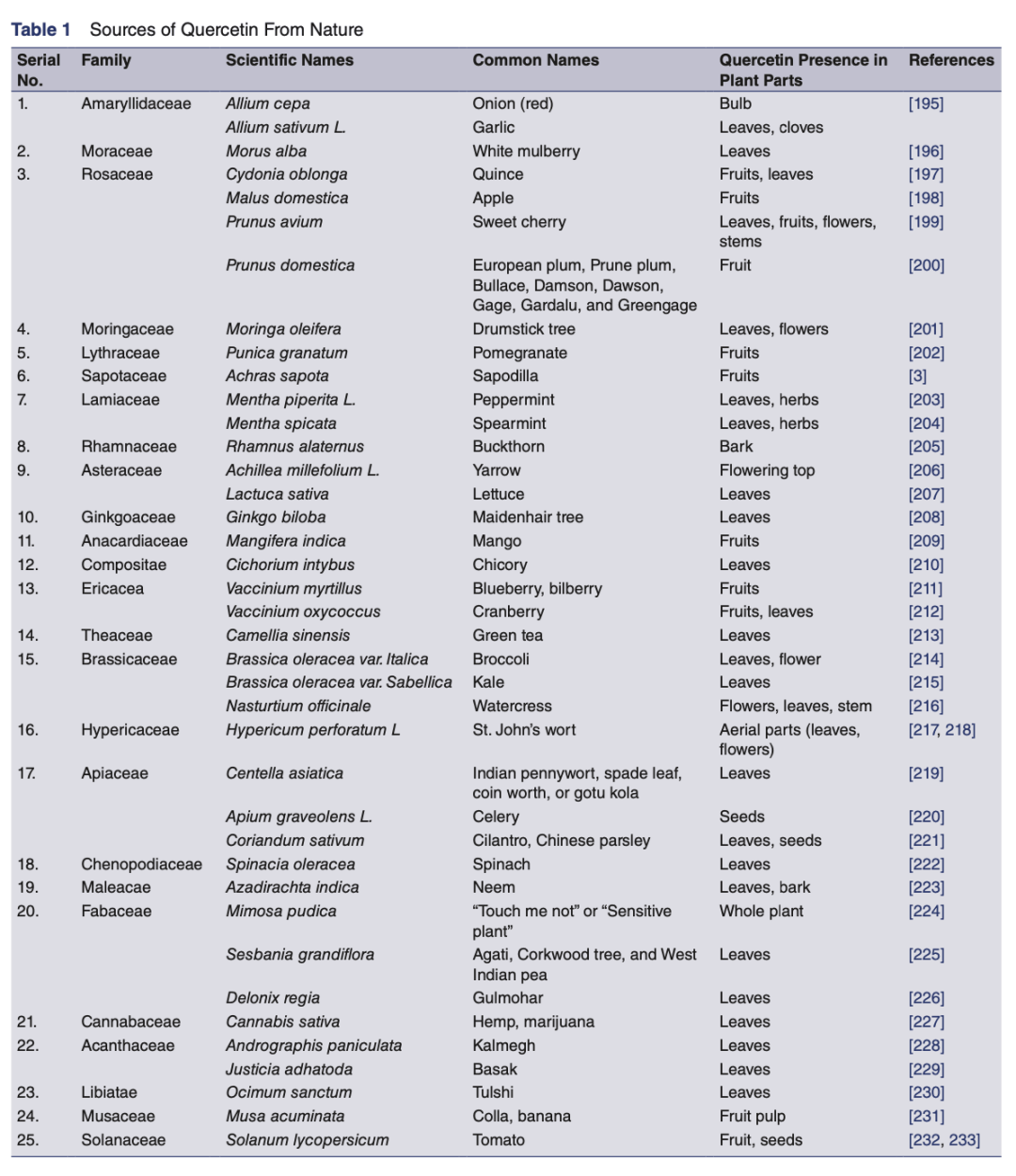
从天然来源到临床应用:槲皮素的药代学挑战与毒理学问题 槲皮素是一种来源非常广泛的黄酮类化合物,几乎遍布我们的日常饮食。苹果、葡萄、蓝莓、洋葱、西兰花、番茄,以及茶叶和一些药用植物里都含有丰富的槲皮素。这意味着我们每天都在不知不觉中摄入槲皮素,它天然安全、容易获得,因此长期以来一直被认为是一种潜在的“功能性营养分子”。 但是,吃进去并不代表身体能有效利用。槲皮素存在一个关键问题:生物利用度很低。由于它本身水溶性差,在胃肠道中吸收效率很低;同时,它会在肝脏和肠道被快速代谢(如葡萄糖醛酸化、硫酸化),导致血浆中实际能检测到的槲皮素浓度远低于实验研究中需要的水平。也就是说,单靠膳食补充,想达到发挥神经保护作用的剂量几乎不可能。 为突破这一瓶颈,研究者开发了纳米制剂、脂质体、聚乙二醇修饰、鼻腔递送等新策略。尤其是鼻腔途径,可以绕过血脑屏障,直接进入中枢神经系统,成为未来重要方向。些技术的共同目标,就是让槲皮素真正“到达病灶”,而不是在胃肠道或肝脏就被消耗掉。 除了吸收问题,剂量安全性也是必须面对的挑战。文章强调,槲皮素是一把“双刃剑”:在低至中等剂量时,它表现出抗氧化、抗炎、保护线粒体的积极效果;但在高剂量下,却可能出现促氧化效应,导致线粒体膜损伤、DNA损伤,甚至触发细胞凋亡。 这意味着,槲皮素的作用高度依赖剂量和使用方式,既不能摄入不足以发挥作用,也不能盲目增加剂量,否则可能“适得其反”。因此,未来如果槲皮素要进入临床治疗,必须建立清晰的剂量—效应关系,并通过药代学/毒理学研究来划定安全范围。 综合来看,槲皮素的“来源广泛”与“利用困难、安全性敏感”形成了鲜明对比。如何在这两者之间找到平衡,是它能否真正走向临床应用的关键。
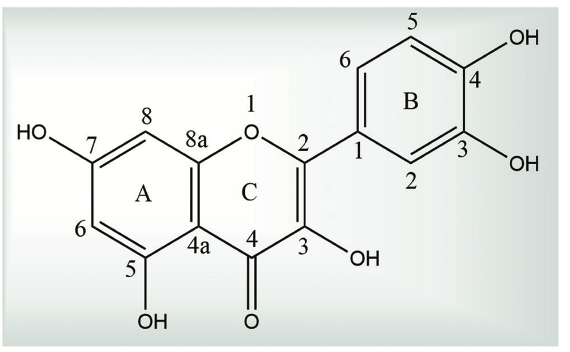
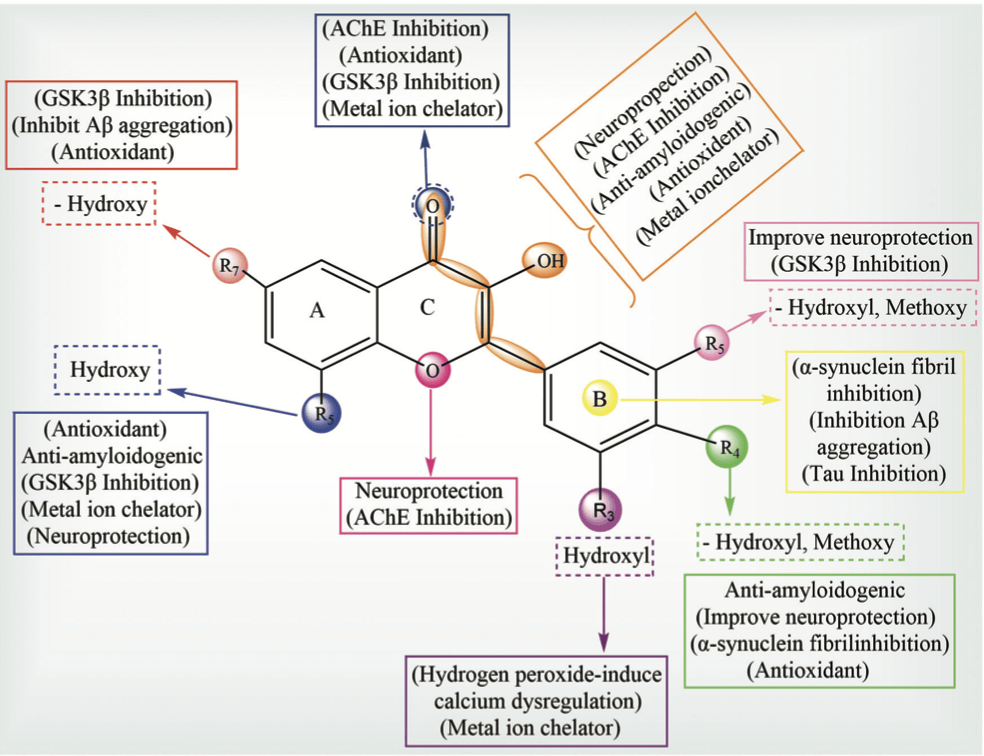
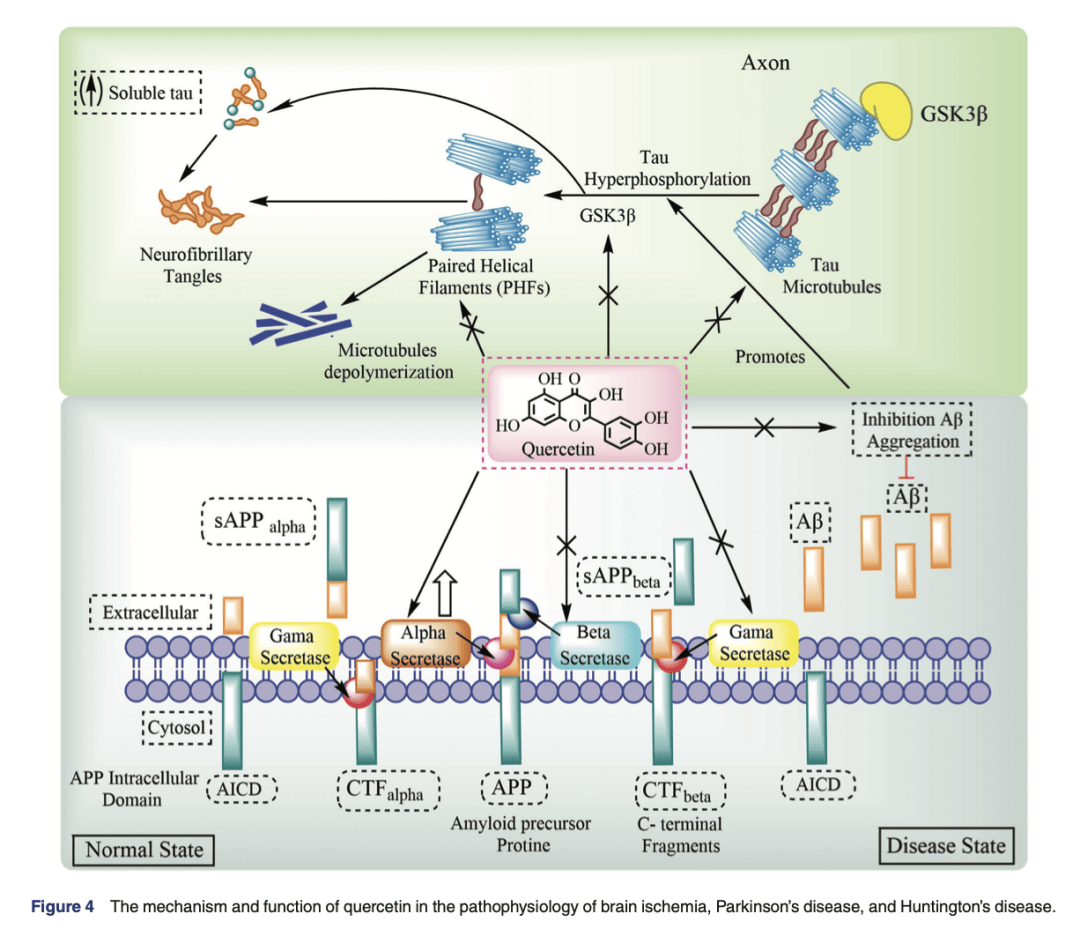
槲皮素的分子基础与构效关系解析 槲皮素属于黄酮醇类化合物,其分子骨架由C6-C3-C6结构单元组成,含有多个关键的羟基取代基与共轭双键。这些结构特征赋予了槲皮素多方面的生物学活性:一方面,其B环上的儿茶酚基团和C环上的4-酮基与2,3-双键能高效清除自由基并螯合过渡金属离子,从而在抗氧化和减少Fenton反应中发挥作用;另一方面,羟基的分布使其能够与蛋白质形成氢键,阻止Aβ肽和α-synuclein等病理性聚集蛋白形成纤维化结构。
药代动力学研究显示,槲皮素的口服生物利用度偏低,主要归因于其水溶性差及在胃肠道和肝脏内的快速代谢(葡萄糖醛酸化、硫酸化和甲基化)。因此,在临床应用中难以达到实验所需的有效浓度。为突破这一限制,研究者开发了多种改良策略,包括纳米制剂、脂质体、聚乙二醇修饰及鼻腔递送等,这些方式能够改善槲皮素的溶解性与稳定性,提高其血脑屏障穿透率和在中枢神经系统内的有效分布。 构效关系(SAR)的研究进一步揭示了槲皮素的神经保护潜力。不同取代基的位置和数量决定了其在多种病理环节中的作用强度:3′,4′-二羟基结构对抗氧化和金属螯合作用至关重要;C环的羰基和共轭双键有利于电子离域,增强自由基清除能力;其他取代基则与抑制炎症反应和维持线粒体功能密切相关。这种独特的化学特征,使槲皮素能够在抗氧化、抗炎、抑制蛋白聚集、保护线粒体和抗凋亡等多个方面同时发挥作用,展现出“多靶点、多机制”的神经保护特性。
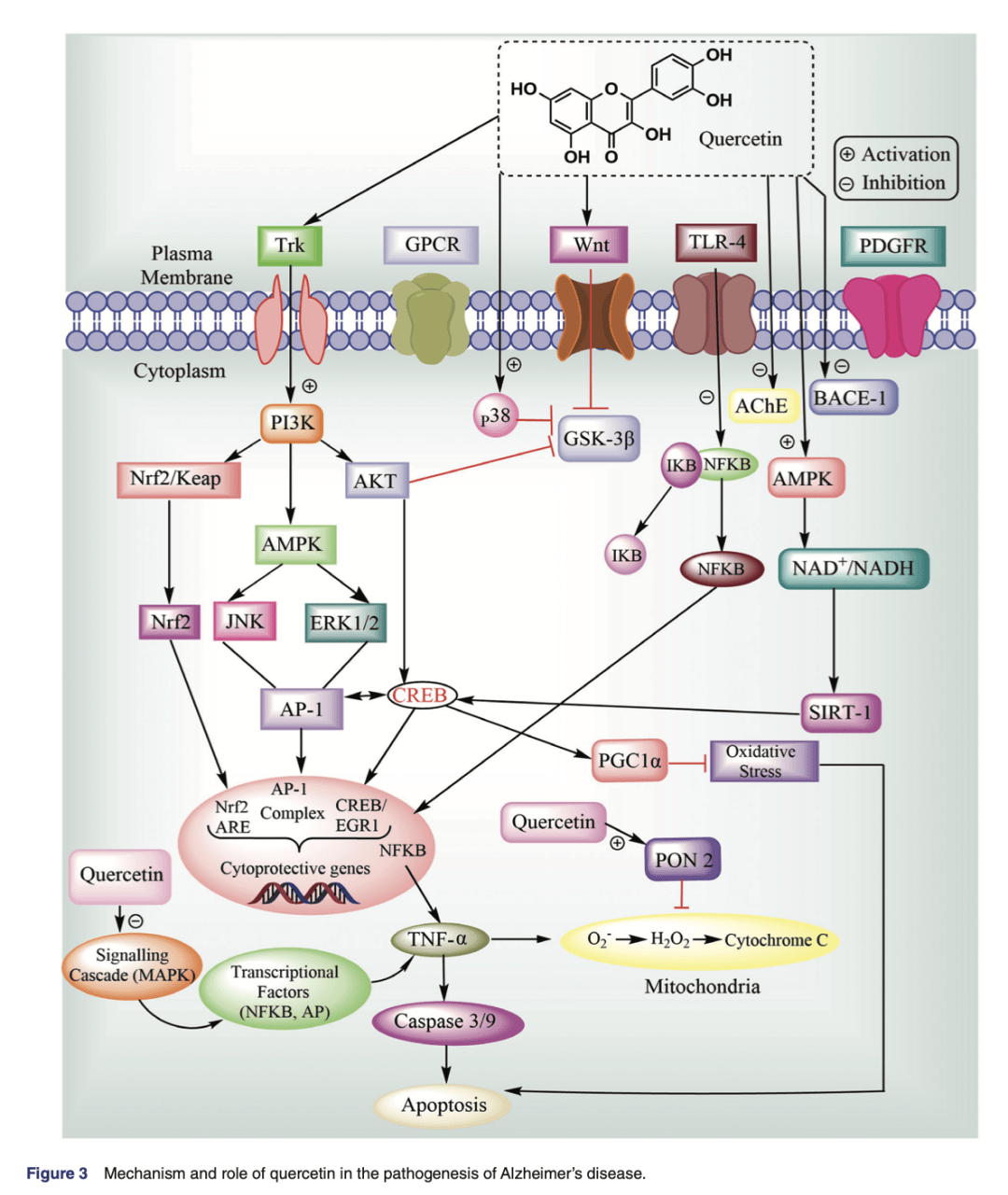
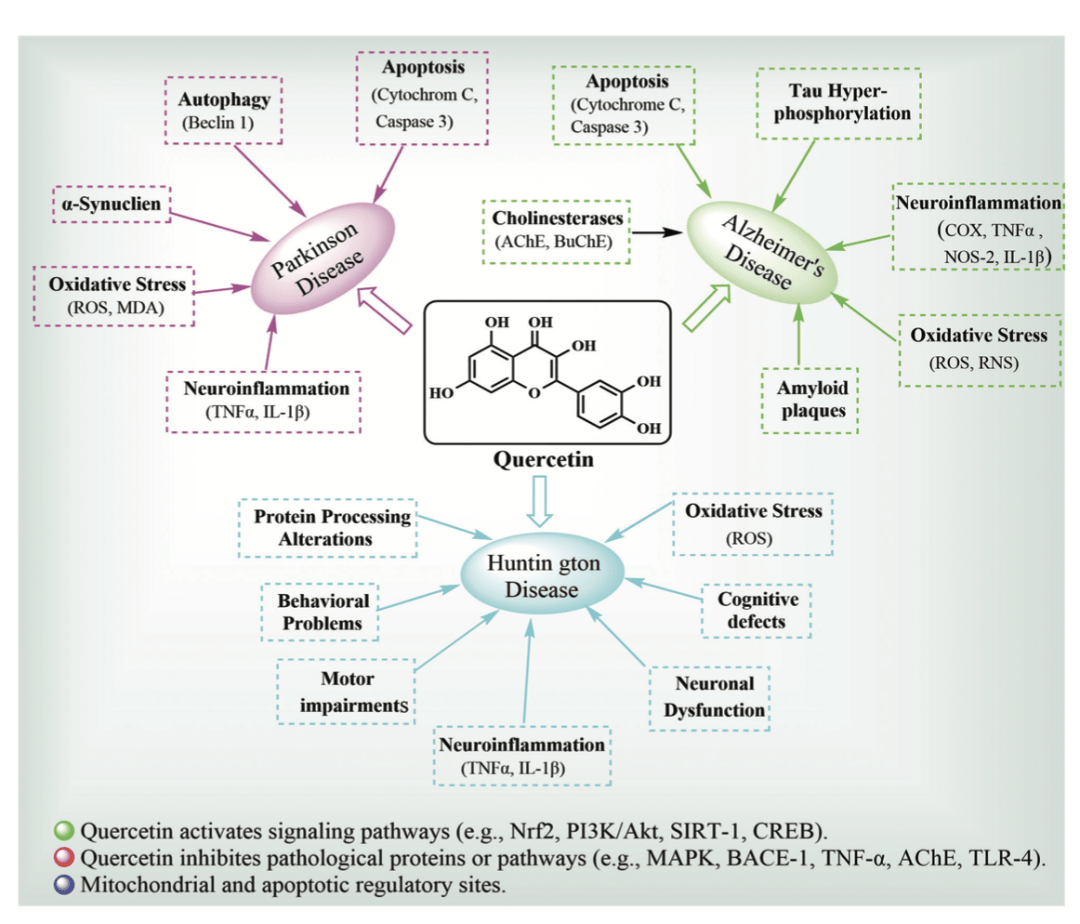
槲皮素在神经退行性疾病中的多机制协同作用 槲皮素能够在神经退行性疾病中发挥广泛的神经保护作用,首先得益于其抗氧化与抗炎特性。它通过激活Nrf2-ARE通路提升抗氧化酶水平,有效清除ROS与RNS;同时,通过抑制NF-κB和MAPK信号减少促炎因子释放,从而减轻神经炎症环境对神经元的损伤。 在能量代谢与细胞稳态方面,槲皮素通过激活PI3K/Akt通路促进线粒体生物合成,维持ATP合成与膜电位稳定,这对高度依赖能量的神经元至关重要。同时,它能阻止Aβ、α-synuclein及mHTT等病理蛋白的异常聚集,减少由蛋白质折叠错误引发的神经毒性。 进一步地,槲皮素还可调控凋亡与神经递质水平。通过抑制caspase-3/-9和JNK/p38信号通路,它降低了细胞凋亡率,保护神经元存活;与此同时,其对乙酰胆碱酯酶的抑制作用提升了乙酰胆碱浓度,有助于改善学习和认知功能。由此可见,槲皮素几乎覆盖了神经退行性疾病的多个核心病理过程,展现出典型的“多靶点、多机制”特征。
槲皮素的神经保护与血管内皮调控效应 大量基础与动物实验研究表明,槲皮素在多种神经退行性疾病模型中都展现出积极疗效。其多靶点特性使其能够同时作用于阿尔茨海默病(AD)、帕金森病(PD)、亨廷顿病(HD)等疾病的关键病理环节。例如,在AD模型中,槲皮素能够减少Aβ沉积、抑制Tau蛋白过度磷酸化并改善认知功能;在PD中,它能抑制多巴胺能神经元损伤、降低α-synuclein聚集;在HD中,则表现出减轻神经毒性和运动障碍的效果。这些证据共同支持槲皮素作为一种广谱的神经保护剂,具有潜在的临床转化价值。 除直接作用于神经元外,槲皮素在维持血管内皮功能和神经血管单元稳态方面同样发挥关键作用。研究表明,槲皮素可通过改善内皮细胞的抗氧化防御和抑制炎症反应,增强一氧化氮(NO)合成,促进血管舒张,进而改善脑血流灌注。同时,它能够保护血脑屏障完整性,减少炎症因子和有害分子进入中枢神经系统,从而降低神经炎症和继发损伤。由此可见,槲皮素不仅是神经元的直接保护剂,还通过调控血管和血脑屏障功能,为神经退行性疾病提供了额外的防护机制。
槲皮素靶向信号通路的神经保护作用 槲皮素的神经保护潜力在很大程度上依赖于对多条关键信号通路的调控。研究表明,它能够激活 Nrf2/ARE 抗氧化通路,增强下游抗氧化酶如HO-1、NQO1和GSH的表达,减轻氧化应激对神经元的损伤。同时,它还能抑制 NF-κB 和 MAPK 通路 的过度活化,从而降低炎症因子的释放,改善神经炎症微环境。在能量代谢方面,槲皮素通过调控 PI3K/Akt/mTOR 和 AMPK 通路,促进线粒体生成和自噬清除异常蛋白,维持神经元能量稳态。这些作用共同缓解了神经退行性疾病中普遍存在的氧化应激、炎症和代谢失衡。
现有研究表明,槲皮素在体外模型和初步临床试验中均展现出神经保护潜力。在多种细胞模型中,它能有效减轻Aβ与α-synuclein诱导的毒性反应,降低ROS生成,抑制炎症因子释放,并改善线粒体功能和细胞存活,验证了其多靶点作用机制。而在临床层面,尽管相关试验数量有限,已有研究提示槲皮素可改善认知功能、增强抗氧化防御并减轻炎症状态。但由于其口服生物利用度低、最佳剂量尚不明确,目前临床应用仍受到限制,未来需要更多大样本和标准化的临床研究来进一步确认其有效性与安全性。 本综述全面梳理了槲皮素在神经退行性疾病中的研究进展。作为一种天然黄酮醇,槲皮素凭借多靶点作用机制,在抗氧化、抗炎、蛋白聚集抑制及血管保护等方面展现出广阔潜力。虽然其临床应用仍受生物利用度等限制,但文章指出,随着新型递药技术和更多临床试验的推进,槲皮素有望成为未来神经退行性疾病的重要候选药物。 引用方式: Debnath I, Ghosh S,Jha SK et al. Mechanistic Insights and Therapeutic Potential of Quercetin in Neuroprotection: AComprehensive Review of Pathways and Clinical Perspectives. BIO Integration. 2025. Vol. 6(1). DOI: 10.15212/bioi-2025-0073 |

 English
English 日本語
日本語 电话:0512-67621565
电话:0512-67621565 邮箱:info@iseediting.com
邮箱:info@iseediting.com 




 最新消息
最新消息