|
BIOI迷你综述 | 基因治疗—打开神经退行性疾病的“希望之盒”
作者:BIOI 来源: 时间:2025-05-09 访问量: 389 |
|
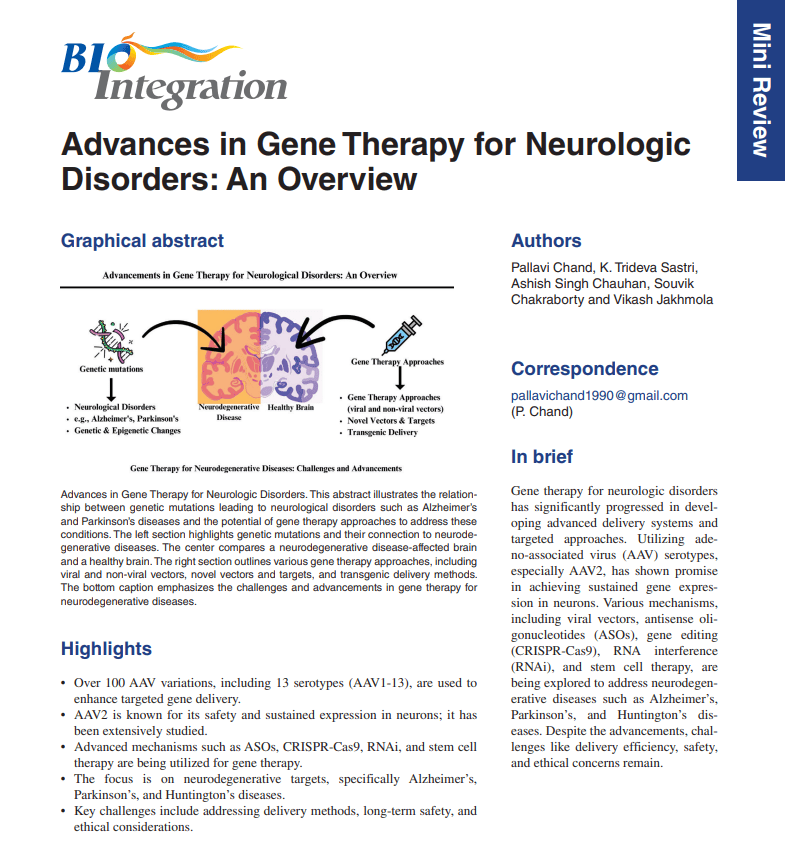
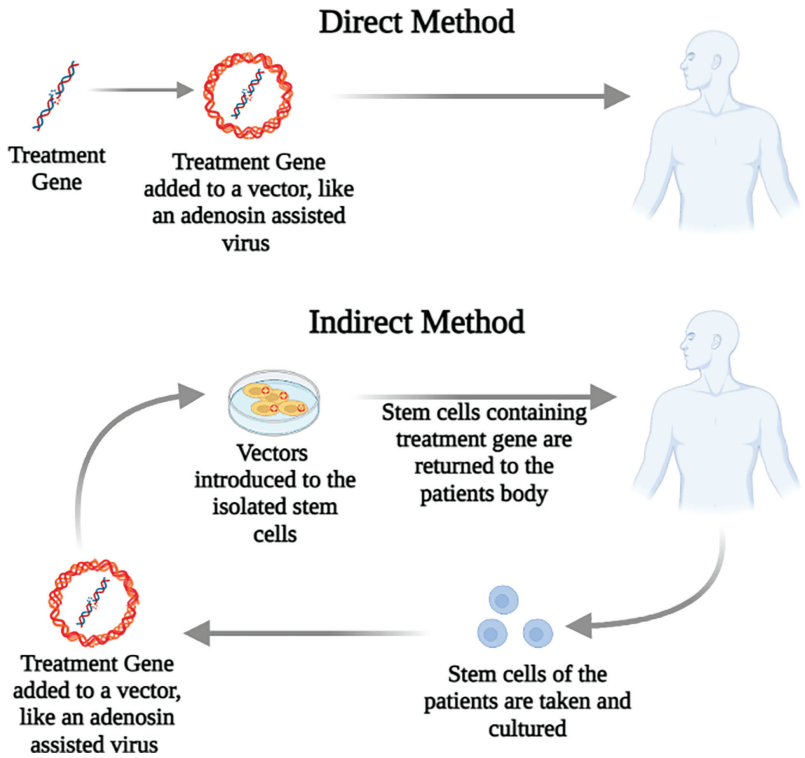
导读—— 全球约1亿人受阿尔茨海默病、帕金森病等神经退行性疾病困扰,传统疗法难以触及疾病根源。随着基因编辑技术(如CRISPR-Cas9)和新型载体的突破,基因治疗正成为改写疾病命运的“钥匙”。通过精准修复致病基因、调控异常蛋白表达,科学家们正跨越血脑屏障的鸿沟,直击神经退行性疾病的“心脏”。本文将结合核心图表,揭示基因治疗如何从实验室迈向临床,为患者点亮希望之光。 近期,BIO Integration上线了一篇Mini Review “Advances in Gene Therapy for Neurologic Disorders: An Overview”。本文综述了神经退行性疾病基因治疗的发展和障碍,并讨论了新的策略、目标以及未来的研究方向。 主要内容 基因治疗的核心在于安全递送治疗性基因至目标脑区,腺相关病毒(AAV)凭借低免疫原性和长效表达优势成为主流载体。非病毒载体如脂质纳米颗粒(LNPs)和阳离子聚合物通过表面修饰可搭载CRISPR或siRNA,在亨廷顿病模型中使突变蛋白表达降低。突破性工程化载体通过静脉注射即可穿透血脑屏障,提高全脑神经元转染率,为广泛性脑部疾病治疗开辟新路径。 图1:神经退行性疾病:挑战和先机 非病毒载体凭借安全性和可设计性崭露头角。阳离子脂质体DOTAP/DOPE复合物可高效包裹siRNA,在亨廷顿病模型中沉默突变HTT基因,使运动障碍缓解;磁性纳米颗粒搭载shRNA通过鼻腔递送,靶向帕金森病模型小鼠的黑质区域,α-突触核蛋白水平下降。外泌体作为天然载体,表面修饰神经元靶向肽后,CRISPR组件递送效率显著提升,且免疫反应近乎为零。近期突破显示,脂质-聚合物杂化载体通过pH响应机制,在脑肿瘤微环境中精准释放基因药物,肿瘤体积缩小。 图2:基因治疗的方法 基因治疗已从概念验证迈向临床转化。AAV9-miHTT注射至亨廷顿病模型羊的纹状体,6个月后突变蛋白减少50%—80%,且正常HTT蛋白未受影响;CRISPR-Cas9编辑技术在小鼠模型中永久性沉默亨廷顿致病基因,显著缓解运动障碍。一项随机对照临床试验中,AAV-GDNF疗法尽管在统计意义未显示出显著优势,但部分帕金森患者有明确临床改善,尤其是特定年龄和病程较长的帕金森患者群体。值得关注的是,锌指蛋白转录因子(ZFP-TFs)在患者神经元中特异性抑制>99%的致病等位基因,正常基因表达保留86%,为精准编辑树立新标杆。 图3:基因治疗基础流程 总结: 尽管基因治疗在神经疾病中取得突破,载体效率、长期安全性仍是核心挑战。未来,AI驱动的载体设计将加速开发周期——机器学习已预测出AAV衣壳新变体,脑靶向效率提升;而碱基编辑技术无需切断DNA双链,大幅降低脱靶风险。随着15项神经疾病基因疗法进入III期临床,一个“修复基因、逆转病程”的新时代正在开启。 引用方式: Chand P, Sastri KT, Chauhan AS et al. Advances in Gene Therapy for Neurologic Disorders: An Overview. BIO Integration. 2025. Vol. 6(1). DOI: 10.15212/bioi-2024-0060 了解更多相关内容,请点击“阅读原文”或复制下方原文链接: https://www.scienceopen.com/hosted-document?doi=10.15212/bioi-2024-0060 |

 English
English 日本語
日本語 电话:0512-67621565
电话:0512-67621565 邮箱:info@iseediting.com
邮箱:info@iseediting.com 




 最新消息
最新消息